De retour à l'école, assis en cours de chimie, nous nous souvenons tous de la table accrochée au mur de la classe ou du laboratoire de chimie. Ce tableau contenait la classification de tout ce qui est connu de l'humanité éléments chimiques, ces composants fondamentaux qui composent la Terre et l'Univers tout entier. Alors nous ne pouvions même pas penser que table de Mendeleïev sans aucun doute l'une des plus grandes découvertes scientifiques, qui est le fondement de nos connaissances modernes de la chimie.
Tableau périodique des éléments chimiques de D. I. Mendeleev
À première vue, son idée semble d'une simplicité trompeuse : organiser éléments chimiques par ordre croissant de poids de leurs atomes. De plus, dans la plupart des cas, il s'avère que les produits chimiques et propriétés physiques de chaque élément sont similaires à l'élément précédent dans le tableau. Ce modèle se manifeste pour tous les éléments, à l'exception des tout premiers, simplement parce qu'ils n'ont pas d'éléments devant eux qui leur sont similaires en poids atomique. C'est grâce à la découverte d'une telle propriété que nous pouvons placer une séquence linéaire d'éléments dans un tableau très semblable à un calendrier mural, et ainsi combiner un grand nombre de types d'éléments chimiques sous une forme claire et cohérente. Bien sûr, on utilise aujourd'hui la notion de numéro atomique (le nombre de protons) pour ordonner le système d'éléments. Cela a aidé à résoudre le soi-disant problème technique de "paire de permutations", mais n'a pas conduit à un changement radical dans la forme du tableau périodique.
V tableau périodique tous les éléments sont classés en fonction de leur numéro atomique, de leur configuration électronique et de leur répétition propriétés chimiques... Les lignes d'un tableau sont appelées périodes et les colonnes sont appelées groupes. Le premier tableau, daté de 1869, ne contenait que 60 éléments, mais maintenant le tableau a dû être agrandi pour accueillir les 118 éléments que nous connaissons aujourd'hui.
Tableau périodique de Mendeleev systématise non seulement les éléments, mais aussi leurs propriétés les plus diverses. Il suffit souvent à un chimiste d'avoir le Tableau Périodique sous les yeux pour répondre correctement à de nombreuses questions (pas seulement des questions d'examen, mais aussi des questions scientifiques).
L'identifiant YouTube de 1M7iKKVnPJE n'est pas valide.
Droit périodique
Il existe deux formules loi périodique éléments chimiques : classiques et modernes.
Classique, tel que présenté par son découvreur D.I. Mendeleev: les propriétés des corps simples, ainsi que les formes et propriétés des composés d'éléments, dépendent périodiquement des valeurs des poids atomiques des éléments.
Moderne : les propriétés des substances simples, ainsi que les propriétés et les formes des composés d'éléments, dépendent périodiquement de la charge du noyau des atomes d'éléments (nombre ordinal).
Une représentation graphique de la loi périodique est le tableau périodique des éléments, qui est une classification naturelle des éléments chimiques basée sur les changements réguliers des propriétés des éléments à partir des charges de leurs atomes. Les images les plus courantes du tableau périodique des éléments de D.I. Les Mendeleev sont des formes courtes et longues.

Groupes et périodes du système périodique
Par groupes sont appelés rangées verticales dans le système périodique. Dans les groupes, les éléments sont combinés selon l'état d'oxydation le plus élevé dans les oxydes. Chaque groupe se compose d'un sous-groupe principal et d'un sous-groupe secondaire. Les principaux sous-groupes comprennent des éléments de petites périodes et des éléments de grandes périodes avec les mêmes propriétés. Les sous-groupes secondaires ne sont constitués que d'éléments de grandes périodes. Les propriétés chimiques des éléments des sous-groupes principal et secondaire diffèrent considérablement.
Point final une rangée horizontale d'éléments est appelée, disposés dans l'ordre croissant des nombres ordinaux (atomiques). Il y a sept périodes dans le système périodique : les première, deuxième et troisième périodes sont appelées petites, elles contiennent respectivement 2, 8 et 8 éléments ; les périodes restantes sont appelées grandes: dans les quatrième et cinquième périodes, il y a 18 éléments chacune, dans la sixième - 32 et dans la septième (encore inachevée) - 31 éléments. Chaque période, sauf la première, commence par un métal alcalin et se termine par un gaz noble.
La signification physique du numéro de sérieélément chimique : le nombre de protons dans le noyau atomique et le nombre d'électrons tournant autour du noyau atomique sont égaux au nombre ordinal de l'élément.
Propriétés du tableau périodique
Rappeler que en groupes appelées rangées verticales dans le système périodique et les propriétés chimiques des éléments des sous-groupes principal et secondaire diffèrent considérablement.
Les propriétés des éléments des sous-groupes changent naturellement de haut en bas :
- propriétés métalliques accrues et non métalliques affaiblis;
- le rayon atomique augmente ;
- la force des bases et des acides anoxiques formés par l'élément augmente ;
- l'électronégativité chute.
Tous les éléments, à l'exception de l'hélium, du néon et de l'argon, forment des composés oxygénés ; il n'y a que huit formes de composés oxygénés. Dans le système périodique, ils sont souvent représentés par des formules générales situées sous chaque groupe dans l'ordre croissant de l'état d'oxydation des éléments : R 2 O, RO, R 2 O 3, RO 2, R 2 O 5, RO 3, R 2 O 7, RO 4, où le symbole R désigne un élément de ce groupe. Les formules d'oxyde plus élevées se réfèrent à tous les éléments d'un groupe, sauf dans des cas exceptionnels où les éléments ne présentent pas un état d'oxydation égal au numéro de groupe (par exemple, le fluor).
Les oxydes de composition R 2 O présentent de fortes propriétés basiques, et leur basicité augmente avec l'augmentation du numéro d'ordre, les oxydes de composition RO (à l'exception de BeO) présentent des propriétés basiques. Les oxydes de composition RO 2, R 2 O 5, RO 3, R 2 O 7 présentent des propriétés acides et leur acidité augmente avec l'augmentation du numéro de série.
Les éléments des sous-groupes principaux, à partir du groupe IV, forment des composés d'hydrogène gazeux. Il existe quatre formes de telles connexions. Ils sont situés sous les éléments des sous-groupes principaux et sont représentés par des formules générales dans la séquence RH 4, RH 3, RH 2, RH.
Les composés RH 4 sont neutres ; RH 3 - faiblement basique ; RH 2 - légèrement acide; RH - Caractère fortement acide.
Rappeler que point final une rangée horizontale d'éléments est appelée, disposés dans l'ordre croissant des nombres ordinaux (atomiques).
Dans une période avec augmentation du nombre ordinal d'un élément :
- l'électronégativité augmente ;
- les propriétés métalliques diminuent, les propriétés non métalliques augmentent ;
- le rayon atomique diminue.

Éléments du tableau périodique
Éléments alcalins et alcalino-terreux
Ceux-ci incluent des éléments des premier et deuxième groupes du tableau périodique. Métaux alcalins du premier groupe - métaux mous, argentés, bien coupés au couteau. Ils ont tous un seul électron sur la coque externe et réagissent parfaitement. Métaux alcalino-terreux du deuxième groupe ont également une teinte argentée. Au niveau externe, deux électrons sont placés et, par conséquent, ces métaux sont moins disposés à interagir avec d'autres éléments. Par rapport aux métaux alcalins, les métaux alcalino-terreux fondent et bout à des températures plus élevées.
Afficher/Masquer le texte
Lanthanides (éléments des terres rares) et actinides
Lanthanides est un groupe d'éléments trouvés à l'origine dans les minéraux rares ; d'où leur nom d'éléments "terres rares". Par la suite, il s'est avéré que ces éléments ne sont pas aussi rares qu'ils le pensaient initialement, et c'est pourquoi le nom de lanthanides a été attribué aux éléments des terres rares. Lanthanides et actinides occupent deux blocs, qui sont situés sous le tableau principal des éléments. Les deux groupes comprennent les métaux ; tous les lanthanides (à l'exception du prométhium) sont non radioactifs ; les actinides, en revanche, sont radioactifs.
Afficher/Masquer le texte
Halogènes et gaz rares
Les halogènes et les gaz rares sont regroupés dans les groupes 17 et 18 du tableau périodique. Halogènes sont des éléments non métalliques, ils ont tous sept électrons dans leur enveloppe externe. V gaz nobles tous les électrons sont dans la couche externe, ils participent donc à peine à la formation de composés. Ces gaz sont appelés « gaz nobles » car ils réagissent rarement avec d'autres éléments ; c'est-à-dire qu'ils se réfèrent aux représentants de la caste noble, qui ont traditionnellement évité les autres personnes dans la société.
Afficher/Masquer le texte
Métaux de transition
Métaux de transition occupent les groupes 3-12 sur le tableau périodique. La plupart d'entre eux sont denses, solides, avec une bonne conductivité électrique et thermique. Leurs électrons de valence (avec lesquels ils se lient à d'autres éléments) sont dans plusieurs couches d'électrons.
Afficher/Masquer le texte
| Métaux de transition |
| Scandium Sc 21 |
| Titane Ti 22 |
| Vanadium V23 |
| Chrome Cr 24 |
| Manganèse Mn 25 |
| Fer Fe 26 |
| Cobalt 27 |
| Nickel Ni28 |
| Cuivre Cu 29 |
| Zinc Zn 30 |
| Yttrium Y 39 |
| Zirconium Zr 40 |
| Niobium Nb 41 |
| Molybdène Mo 42 |
| Technétium Tc 43 |
| Ruthénium Ru 44 |
| Rhodium Rh 45 |
| Palladium Pd 46 |
| Argent Ag 47 |
| Cadmium Cd 48 |
| Lu 71 |
| Hafnium Hf 72 |
| Tantale Ta 73 |
| Tungstène W 74 |
| Rhénium Re 75 |
| Osmium Os 76 |
| Iridium Ir 77 |
| Platine Pt 78 |
| Or Au 79 |
| Mercure Hg 80 |
| Laurent Lr 103 |
| Rutherfordium Rf 104 |
| Dubnium Db 105 |
| Seaborgium Sg 106 |
| Borium Bh 107 |
| Hassius Hs 108 |
| Meitnerium Mt 109 |
| Darmstadty Ds 110 |
| Rayon X Rg 111 |
| Copernicium Cn 112 |
Métalloïdes
Métalloïdes occupent les groupes 13-16 du tableau périodique. Les métalloïdes tels que le bore, le germanium et le silicium sont des semi-conducteurs utilisés pour fabriquer des puces informatiques et des circuits imprimés.
Afficher/Masquer le texte
Métaux post-transition
Éléments appelés métaux post-transition, appartiennent aux groupes 13-15 du tableau périodique. Contrairement aux métaux, ils n'ont pas de brillant, mais ont une couleur mate. En comparaison avec les métaux de transition, les métaux de post-transition sont plus doux, ont plus basse température fusion et ébullition, électronégativité plus élevée. Leurs électrons de valence, avec lesquels ils attachent d'autres éléments, ne sont situés que sur la couche externe d'électrons. Les éléments du groupe des métaux de post-transition ont beaucoup plus forte fièvre bouillant que les métalloïdes.
Consolidez maintenant vos connaissances en regardant une vidéo sur le tableau périodique et plus encore.
Génial, le premier pas vers la connaissance est fait. Maintenant, vous êtes plus ou moins guidé par le tableau périodique et il vous sera très utile, car le tableau périodique est le fondement sur lequel repose cette science étonnante.
Si vous trouvez le tableau périodique difficile à comprendre, vous n'êtes pas seul ! Bien qu'il puisse être difficile de comprendre ses principes, savoir comment l'utiliser vous aidera dans vos études scientifiques. Tout d'abord, étudiez la structure du tableau et les informations que vous pouvez en tirer sur chaque élément chimique. Ensuite, vous pouvez commencer à explorer les propriétés de chaque élément. Et enfin, en utilisant le tableau périodique, vous pouvez déterminer le nombre de neutrons dans un atome d'un élément chimique particulier.
Pas
Partie 1
Structure du tableau- Par exemple, la première ligne du tableau contient de l'hydrogène, qui a le numéro atomique 1, et de l'hélium, qui a le numéro atomique 2. Cependant, ils sont situés sur des bords opposés, car ils appartiennent à des groupes différents.
-
Renseignez-vous sur les groupes qui incluent des éléments ayant des propriétés physiques et chimiques similaires. Les éléments de chaque groupe sont disposés dans une colonne verticale correspondante. Ils sont généralement représentés par une seule couleur, ce qui permet d'identifier les éléments ayant des propriétés physiques et chimiques similaires et de prédire leur comportement. Tous les éléments d'un groupe particulier ont le même nombre d'électrons sur la couche externe.
- L'hydrogène peut être attribué à la fois au groupe des métaux alcalins et au groupe des halogènes. Dans certains tableaux, il est indiqué dans les deux groupes.
- Dans la plupart des cas, les groupes sont numérotés de 1 à 18 et les numéros sont placés en haut ou en bas du tableau. Les nombres peuvent être spécifiés en chiffres romains (par exemple, IA) ou arabes (par exemple, 1A ou 1).
- Se déplacer le long de la colonne de haut en bas est dit « visualiser le groupe ».
-
Découvrez pourquoi il y a des cellules vides dans le tableau. Les éléments sont classés non seulement en fonction de leur numéro atomique, mais également en fonction de groupes (les éléments d'un groupe ont des propriétés physiques et chimiques similaires). Cela permet de mieux comprendre le comportement d'un élément particulier. Cependant, avec la croissance du numéro atomique, les éléments qui tombent dans le groupe correspondant ne sont pas toujours trouvés, par conséquent, il y a des cellules vides dans le tableau.
- Par exemple, les 3 premières rangées ont des cellules vides, car les métaux de transition ne se trouvent qu'à partir du numéro atomique 21.
- Les éléments portant les numéros atomiques 57 à 102 sont classés comme éléments des terres rares et sont généralement répertoriés dans un sous-groupe distinct dans le coin inférieur droit du tableau.
-
Chaque ligne du tableau représente une période. Tous les éléments de la même période ont le même numéro orbitales atomiques, sur lequel se trouvent les électrons dans les atomes. Le nombre d'orbitales correspond au numéro de la période. Le tableau contient 7 lignes, soit 7 périodes.
- Par exemple, les atomes des éléments de la première période ont une orbitale et les atomes des éléments de la septième période ont 7 orbitales.
- En règle générale, les périodes sont indiquées par des chiffres de 1 à 7 à gauche du tableau.
- Se déplacer le long de la ligne de gauche à droite est dit « visualiser une période ».
-
Apprenez à distinguer les métaux, les métalloïdes et les non-métaux. Vous comprendrez mieux les propriétés d'un élément si vous pouvez déterminer à quel type il appartient. Pour plus de commodité, dans la plupart des tableaux, les métaux, les métalloïdes et les non-métaux sont désignés Couleurs différentes... Les métaux sont à gauche et les non-métaux sont à droite du tableau. Les métalloïdes sont situés entre eux.
Partie 2
Désignations des éléments-
Chaque élément est désigné par une ou deux lettres latines. En règle générale, le symbole de l'élément est affiché en grosses lettres au centre de la cellule correspondante. Un symbole est un nom abrégé pour un élément, qui est le même dans la plupart des langues. Lorsque vous faites des expériences et travaillez avec des équations chimiques, les symboles des éléments sont couramment utilisés, il est donc utile de s'en souvenir.
- En règle générale, les symboles des éléments sont une abréviation de leur nom latin, bien que pour certains, en particulier les éléments récemment découverts, ils soient dérivés d'un nom commun. Par exemple, l'hélium est désigné par le symbole He, qui est proche du nom commun dans la plupart des langues. En même temps, le fer est désigné par Fe, qui est une abréviation de son nom latin.
-
Faites attention au nom complet de l'élément s'il apparaît dans le tableau. Ce "nom" de l'élément est utilisé dans le texte normal. Par exemple, « hélium » et « carbone » sont les noms des éléments. Habituellement, mais pas toujours, les noms complets des éléments sont répertoriés sous leur symbole chimique.
- Parfois, les noms des éléments ne sont pas indiqués dans le tableau et seuls leurs symboles chimiques sont indiqués.
-
Trouvez le numéro atomique. Habituellement, le numéro atomique d'un élément est situé en haut de la cellule correspondante, au milieu ou dans le coin. Il peut également apparaître sous le nom du symbole ou de l'élément. Les éléments ont des numéros atomiques de 1 à 118.
- Le numéro atomique est toujours un entier.
-
Rappelez-vous que le numéro atomique correspond au nombre de protons dans l'atome. Tous les atomes d'un élément contiennent le même nombre de protons. Contrairement aux électrons, le nombre de protons dans les atomes d'un élément reste constant. Sinon, un autre élément chimique serait apparu !
-
Le tableau périodique, ou le tableau périodique des éléments chimiques, commence dans le coin supérieur gauche et se termine à la fin de la dernière ligne du tableau (dans le coin inférieur droit). Les éléments du tableau sont classés de gauche à droite par ordre croissant de leur numéro atomique. Le numéro atomique indique le nombre de protons dans un atome. De plus, avec une augmentation du numéro atomique, la masse atomique augmente également. Ainsi, par l'emplacement d'un élément dans le tableau périodique, vous pouvez déterminer sa masse atomique.
Comme vous pouvez le voir, chaque élément suivant contient un proton de plus que l'élément qui le précède. C'est évident quand on regarde les numéros atomiques. Les nombres atomiques augmentent de un lorsque vous vous déplacez de gauche à droite. Étant donné que les éléments sont organisés en groupes, certaines cellules du tableau restent vides.
Comment utiliser le tableau périodique Pour un non-initié, lire le tableau périodique revient à regarder les anciennes runes des elfes pour un gnome. Et le tableau périodique, en passant, s'il est utilisé correctement, peut en dire beaucoup sur le monde. Outre le fait qu'il vous sera utile lors de l'examen, il est également tout simplement irremplaçable pour résoudre un grand nombre de problèmes chimiques et physiques. Mais comment le lire ? Heureusement, aujourd'hui, tout le monde peut apprendre cet art. Cet article va vous montrer comment comprendre le tableau périodique.
Le tableau périodique des éléments chimiques (tableau périodique) est une classification des éléments chimiques, qui établit la dépendance de diverses propriétés des éléments sur la charge du noyau atomique.
Histoire de la création d'une table
Dmitry Ivanovich Mendeleev n'était pas un simple chimiste, si l'on en croit. Il était chimiste, physicien, géologue, métrologue, écologiste, économiste, pétrolier, aéronaute, luthier et enseignant. Au cours de sa vie, le scientifique a réussi à mener de nombreuses recherches fondamentales dans divers domaines de la connaissance. Par exemple, il est largement admis que c'est Mendeleev qui a calculé la force idéale de la vodka - 40 degrés. Nous ne savons pas ce que Mendeleev pensait de la vodka, mais nous savons avec certitude que sa thèse sur le thème "Discours sur la combinaison de l'alcool et de l'eau" n'avait rien à voir avec la vodka et considérait des concentrations d'alcool à partir de 70 degrés. Avec tous les mérites du scientifique, la découverte de la loi périodique des éléments chimiques - l'une des lois fondamentales de la nature, lui a valu la plus grande renommée.

Il existe une légende selon laquelle un scientifique a rêvé du système périodique, après quoi il n'a eu qu'à affiner l'idée qui est apparue. Mais, si tout était si simple .. Cette version de la création du tableau périodique n'est apparemment rien de plus qu'une légende. Lorsqu'on lui a demandé comment la table avait été ouverte, Dmitry Ivanovich lui-même a répondu : " J'y pense depuis peut-être vingt ans, mais vous pensez : j'étais assis et du coup... c'est fait.»
Au milieu du XIXe siècle, des tentatives d'ordonnancement des éléments chimiques connus (63 éléments étaient connus) ont été entreprises simultanément par plusieurs scientifiques. Par exemple, en 1862, Alexander Émile Chancourtua a placé des éléments le long d'une ligne hélicoïdale et a noté la répétition cyclique des propriétés chimiques. Le chimiste et musicien John Alexander Newlands a proposé sa propre version du tableau périodique en 1866. Un fait intéressant est que le scientifique a essayé de trouver une harmonie musicale mystique dans l'arrangement des éléments. Parmi les autres tentatives, il y a eu la tentative de Mendeleev, qui a été couronnée de succès.

En 1869, le premier schéma du tableau est publié, et le 1er mars 1869 est considéré comme le jour de l'ouverture de la loi périodique. L'essence de la découverte de Mendeleev était que les propriétés des éléments avec une augmentation de la masse atomique ne changent pas de manière monotone, mais périodiquement. La première version du tableau ne contenait que 63 éléments, mais Mendeleev a fait un certain nombre de solutions très atypiques. Ainsi, il a deviné de laisser de la place dans le tableau pour les éléments encore non découverts, et a également modifié les masses atomiques de certains éléments. La justesse fondamentale de la loi déduite par Mendeleev a été confirmée très rapidement, après la découverte du gallium, du scandium et du germanium, dont l'existence a été prédite par les scientifiques.
Vue moderne du tableau périodique
Ci-dessous le tableau lui-même
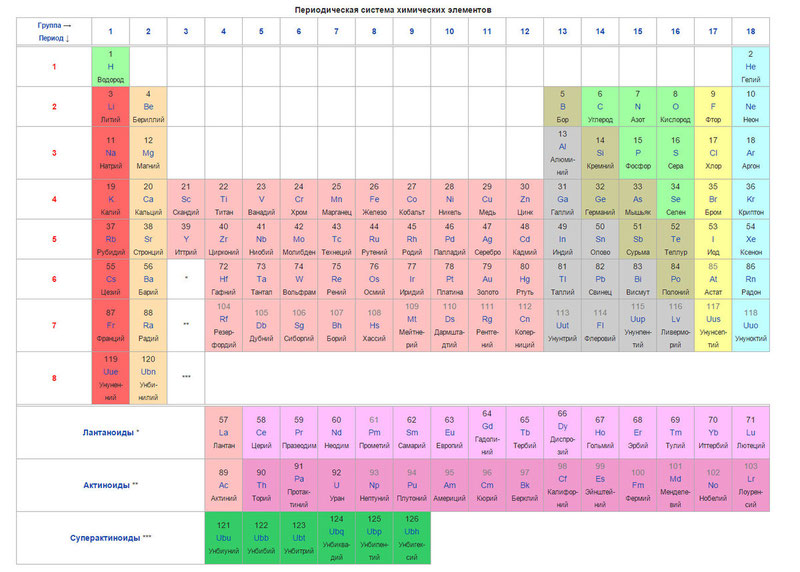
Aujourd'hui, pour ordonner des éléments, au lieu de poids atomique (masse atomique), le concept de numéro atomique (le nombre de protons dans le noyau) est utilisé. Le tableau contient 120 éléments, qui sont situés de gauche à droite par ordre croissant de numéro atomique (nombre de protons)
Les colonnes du tableau sont les soi-disant groupes et les lignes sont les périodes. Il y a 18 groupes et 8 périodes dans le tableau.
- Les propriétés métalliques des éléments diminuent en se déplaçant le long de la période de gauche à droite et augmentent dans la direction opposée.
- La taille des atomes diminue en se déplaçant de gauche à droite le long des périodes.
- En se déplaçant de haut en bas dans le groupe, les propriétés métalliques réductrices augmentent.
- Les propriétés oxydantes et non métalliques augmentent en se déplaçant le long de la période de gauche à droite. Je suis.
Que pouvons-nous apprendre sur un élément de la table? Par exemple, prenons le troisième élément du tableau - le lithium, et considérons-le en détail.

Tout d'abord, nous voyons le symbole de l'élément lui-même et son nom en dessous. Dans le coin supérieur gauche se trouve le numéro atomique de l'élément, dans l'ordre dans lequel l'élément est situé dans le tableau. Le numéro atomique, comme déjà mentionné, est égal au nombre de protons dans le noyau. Le nombre de protons positifs est généralement égal au nombre d'électrons négatifs dans un atome (hors isotopes).
La masse atomique est indiquée sous le numéro atomique (dans cette version du tableau). Si nous arrondissons la masse atomique à l'entier le plus proche, nous obtenons ce qu'on appelle le nombre de masse. La différence entre le nombre de masse et le numéro atomique donne le nombre de neutrons dans le noyau. Ainsi, le nombre de neutrons dans le noyau d'hélium est de deux et dans le lithium de quatre.
Notre cours "Tableau périodique pour les nuls" est donc terminé. En conclusion, nous vous invitons à regarder une vidéo thématique, et nous espérons que la question de savoir comment utiliser le tableau périodique est devenue plus claire pour vous. Nous vous rappelons qu'il est toujours plus efficace d'étudier un nouveau sujet non pas seul, mais avec l'aide d'un mentor expérimenté. C'est pourquoi, vous ne devez jamais oublier ceux qui partageront volontiers leurs connaissances et leur expérience avec vous.
À l'heure actuelle, il contient officiellement 118 produits chimiques. Parmi ceux-ci, 94 se trouvent dans la nature, les 24 restants sont obtenus artificiellement à la suite de réactions nucléaires. De tous les produits chimiques trouvés dans la nature, 88 ; des éléments tels que le technétium Tc, prométhium après-midi, astatine À et france Fr, ainsi que tous les éléments suivant l'uranium U, ont été obtenus artificiellement pour la première fois. Dans des conditions normales, les substances simples correspondantes pour 11 éléments sont des gaz, pour 2 - liquides, pour le reste des éléments - solides.
A lire
 Dmitri Ivanovitch Mendeleïev- Scientifique-encyclopédiste russe, personnalité publique. Chimiste, physicochimiste, physicien, métrologue, économiste, technologue, géologue, météorologue, enseignant, aéronaute, luthier. Professeur de l'Université de Saint-Pétersbourg; Membre correspondant de la catégorie "physique" de l'Académie impériale des sciences de Saint-Pétersbourg. Parmi les découvertes les plus célèbres se trouve la loi périodique des éléments chimiques, l'une des lois fondamentales de l'univers, inhérente à toutes les sciences naturelles.
Dmitri Ivanovitch Mendeleïev- Scientifique-encyclopédiste russe, personnalité publique. Chimiste, physicochimiste, physicien, métrologue, économiste, technologue, géologue, météorologue, enseignant, aéronaute, luthier. Professeur de l'Université de Saint-Pétersbourg; Membre correspondant de la catégorie "physique" de l'Académie impériale des sciences de Saint-Pétersbourg. Parmi les découvertes les plus célèbres se trouve la loi périodique des éléments chimiques, l'une des lois fondamentales de l'univers, inhérente à toutes les sciences naturelles.
Tableau périodique des éléments chimiques- la classification des éléments chimiques, qui établit la dépendance de diverses propriétés des éléments vis-à-vis de la charge du noyau atomique. Le système est une expression graphique de la loi périodique établie par le chimiste russe D.I. Mendeleïev en 1869. Sa version initiale a été développée par D.I. Mendeleev en 1869-1871 et a établi la dépendance des propriétés des éléments sur leur poids atomique. Au total, plusieurs centaines de variantes de l'image du système périodique ont été proposées. V version moderne du système, on suppose que les éléments sont résumés dans un tableau à deux dimensions, dans lequel chaque colonne détermine les propriétés physiques et chimiques de base, et les lignes représentent des périodes, dans une certaine mesure similaires les unes aux autres. Au milieu du 19ème siècle, 63 éléments chimiques avaient été découverts, et des tentatives pour trouver des modèles dans cet ensemble ont été faites à plusieurs reprises. Plus courantes que d'autres sont 3 formes du tableau périodique : "court", "long" et "extra-long". Dans la version « extra-longue », chaque point occupe exactement une ligne. Tableau périodique des D.I. Mendeleev est devenu le jalon le plus important dans le développement de la doctrine atomique-moléculaire.
