Bahkan di sekolah, saat mengikuti pelajaran kimia, kita semua ingat meja di dinding kelas atau laboratorium kimia. Tabel ini berisi klasifikasi semua yang diketahui umat manusia unsur kimia, komponen fundamental yang membentuk Bumi dan seluruh Alam Semesta. Saat itu kami bahkan tidak dapat memikirkan hal itu Tabel Mendeleev tidak diragukan lagi merupakan salah satu penemuan ilmiah terbesar, yang merupakan landasan pengetahuan kimia modern kita.
Tabel periodik unsur kimia D.I.Mendeleev
Sekilas, idenya terlihat sederhana: mengatur unsur kimia berdasarkan pertambahan berat atomnya. Selain itu, dalam banyak kasus ternyata bahan kimia dan properti fisik setiap elemen serupa dengan elemen sebelumnya dalam tabel. Pola ini muncul untuk semua unsur kecuali beberapa unsur pertama, hanya karena unsur-unsur tersebut tidak mempunyai unsur yang serupa dalam berat atomnya. Berkat penemuan sifat inilah kita dapat menempatkan barisan unsur-unsur linier dalam sebuah tabel seperti kalender dinding, dan dengan demikian menggabungkan sejumlah besar jenis unsur kimia dalam bentuk yang jelas dan koheren. Tentu saja, saat ini kita menggunakan konsep nomor atom (jumlah proton) untuk mengurutkan sistem unsur. Hal ini membantu memecahkan apa yang disebut masalah teknis “pasangan permutasi”, namun tidak menyebabkan perubahan mendasar pada tampilan tabel periodik.
DI DALAM tabel periodik semua unsur diurutkan berdasarkan nomor atom, konfigurasi elektron, dan pengulangannya sifat kimia. Baris-baris dalam tabel disebut titik, dan kolom-kolom disebut golongan. Tabel pertama, yang dibuat pada tahun 1869, hanya berisi 60 elemen, namun sekarang tabel tersebut harus diperbesar untuk menampung 118 elemen yang kita kenal sekarang.
Tabel periodik Mendeleev mensistematisasikan tidak hanya unsur-unsurnya, tetapi juga sifat-sifatnya yang paling beragam. Seringkali seorang ahli kimia cukup memiliki Tabel Periodik di depan matanya untuk menjawab banyak pertanyaan dengan benar (tidak hanya soal ujian, tetapi juga soal ilmiah).
ID YouTube 1M7iKKVnPJE tidak valid.
hukum periodik
Ada dua formulasi hukum periodik unsur kimia: klasik dan modern.
Klasik, seperti yang dikemukakan oleh penemunya D.I. Mendeleev: sifat-sifat benda sederhana, serta bentuk dan sifat senyawa unsur, secara periodik bergantung pada nilai berat atom unsur.
Modern: sifat-sifat zat sederhana, serta sifat dan bentuk senyawa unsur, secara periodik bergantung pada muatan inti atom unsur (bilangan urut).
Representasi grafis dari hukum periodik adalah sistem periodik unsur, yang merupakan klasifikasi alami unsur-unsur kimia berdasarkan perubahan teratur sifat-sifat unsur tergantung pada muatan atomnya. Gambar paling umum dari tabel periodik unsur adalah D.I. Bentuk Mendeleev ada yang pendek dan panjang.

Golongan dan periode Tabel Periodik
Dalam kelompok disebut baris vertikal dalam tabel periodik. Dalam golongan, unsur-unsur digabungkan berdasarkan bilangan oksidasi tertinggi dalam oksidanya. Setiap kelompok terdiri dari subkelompok utama dan sekunder. Subkelompok utama mencakup unsur-unsur periode kecil dan unsur-unsur periode besar dengan sifat yang sama. Subkelompok samping hanya terdiri dari unsur-unsur periode besar. Sifat kimia unsur-unsur subkelompok utama dan sekunder berbeda secara signifikan.
Periode disebut barisan mendatar unsur-unsur yang disusun berdasarkan kenaikan nomor atom. Ada tujuh periode dalam sistem periodik: periode pertama, kedua dan ketiga disebut periode kecil, masing-masing mengandung 2, 8 dan 8 unsur; periode yang tersisa disebut besar: pada periode keempat dan kelima ada 18 elemen, pada periode keenam - 32, dan pada periode ketujuh (belum selesai) - 31 elemen. Setiap periode, kecuali periode pertama, dimulai dengan logam alkali dan diakhiri dengan gas mulia.
Arti fisik dari nomor seri unsur kimia: jumlah proton dalam inti atom dan jumlah elektron yang mengelilingi inti atom sama dengan nomor atom unsur tersebut.
Sifat-sifat tabel periodik
Izinkan kami mengingatkan Anda akan hal itu kelompok disebut baris vertikal dalam tabel periodik dan sifat kimia unsur-unsur subkelompok utama dan sekunder berbeda secara signifikan.
Sifat-sifat unsur dalam subkelompok berubah secara alami dari atas ke bawah:
- sifat logam meningkat dan sifat nonlogam melemah;
- jari-jari atom bertambah;
- kekuatan basa dan asam bebas oksigen yang dibentuk oleh unsur tersebut meningkat;
- keelektronegatifan berkurang.
Semua unsur kecuali helium, neon dan argon membentuk senyawa oksigen; hanya ada delapan bentuk senyawa oksigen. Dalam tabel periodik, unsur-unsur tersebut sering digambarkan dengan rumus umum, yang terletak di bawah setiap golongan menurut kenaikan bilangan oksidasi unsur-unsur: R 2 O, RO, R 2 O 3, RO 2, R 2 O 5, RO 3, R 2 O 7, RO 4, dimana simbol R menunjukkan suatu unsur dalam golongan ini. Rumus oksida yang lebih tinggi berlaku untuk semua unsur dalam satu golongan, kecuali dalam kasus luar biasa ketika unsur-unsur tersebut tidak menunjukkan bilangan oksidasi yang sama dengan nomor golongannya (misalnya, fluor).
Oksida dengan komposisi R 2 O menunjukkan sifat basa kuat, dan kebasaannya meningkat seiring dengan bertambahnya nomor atom; oksida dengan komposisi RO (dengan pengecualian BeO) menunjukkan sifat basa. Oksida dari komposisi RO 2, R 2 O 5, RO 3, R 2 O 7 menunjukkan sifat asam, dan keasamannya meningkat seiring dengan bertambahnya nomor atom.
Unsur-unsur subkelompok utama, mulai dari golongan IV, membentuk senyawa gas hidrogen. Ada empat bentuk senyawa tersebut. Mereka terletak di bawah elemen subkelompok utama dan diwakili oleh rumus umum dalam urutan RH 4, RH 3, RH 2, RH.
Senyawa RH 4 bersifat netral; RH 3 - basa lemah; RH 2 - sedikit asam; RH - karakter asam kuat.
Izinkan kami mengingatkan Anda akan hal itu periode disebut barisan mendatar unsur-unsur yang disusun berdasarkan kenaikan nomor atom.
Dalam periode dengan bertambahnya nomor seri elemen:
- keelektronegatifan meningkat;
- sifat logam menurun, sifat nonlogam meningkat;
- jari-jari atom berkurang.

Elemen tabel periodik
Unsur alkali dan alkali tanah
Ini termasuk unsur-unsur dari kelompok pertama dan kedua tabel periodik. Logam alkali dari kelompok pertama - logam lunak, berwarna perak, mudah dipotong dengan pisau. Mereka semua memiliki satu elektron di kulit terluarnya dan bereaksi sempurna. Logam alkali tanah dari kelompok kedua juga memiliki warna keperakan. Dua elektron ditempatkan pada tingkat terluar, dan karenanya, logam-logam ini kurang mudah berinteraksi dengan unsur-unsur lain. Dibandingkan dengan logam alkali, logam alkali tanah meleleh dan mendidih pada suhu yang lebih tinggi.
Tampilkan/Sembunyikan teks
Lantanida (unsur tanah jarang) dan aktinida
Lantanida- sekelompok unsur yang awalnya ditemukan dalam mineral langka; oleh karena itu dinamakan unsur "tanah jarang". Belakangan, ternyata unsur-unsur tersebut tidak selangka yang diperkirakan semula, oleh karena itu nama lantanida diberikan kepada unsur tanah jarang. Lantanida dan aktinida menempati dua blok, yang terletak di bawah tabel elemen utama. Kedua kelompok tersebut termasuk logam; semua lantanida (kecuali promethium) bersifat non-radioaktif; aktinida, sebaliknya, bersifat radioaktif.
Tampilkan/Sembunyikan teks
Halogen dan gas mulia
Halogen dan gas mulia dikelompokkan ke dalam golongan 17 dan 18 tabel periodik. Halogen adalah unsur non-logam, semuanya memiliki tujuh elektron di kulit terluarnya. DI DALAM gas mulia Semua elektron berada di kulit terluar, sehingga mereka sulit berpartisipasi dalam pembentukan senyawa. Gas-gas ini disebut gas “mulia” karena jarang bereaksi dengan unsur lain; artinya, mereka mengacu pada anggota kasta bangsawan yang secara tradisional menjauhi orang lain dalam masyarakat.
Tampilkan/Sembunyikan teks
Logam transisi
Logam transisi menempati golongan 3-12 dalam tabel periodik. Kebanyakan dari mereka padat, keras, dengan konduktivitas listrik dan termal yang baik. Elektron valensinya (yang dengannya mereka bergabung dengan unsur lain) terletak di beberapa kulit elektron.
Tampilkan/Sembunyikan teks
| Logam transisi |
| Skandium Sc 21 |
| Titan Ti 22 |
| Vanadium V 23 |
| Chrome Cr 24 |
| Mangan Mn 25 |
| Besi Fe 26 |
| Kobalt Co 27 |
| Nikel Ni 28 |
| Tembaga Cu 29 |
| Seng Zn 30 |
| Itrium Y 39 |
| Zirkonium Zr 40 |
| Niobium Nb 41 |
| Molibdenum Mo 42 |
| Teknesium Tc 43 |
| Rutenium Ru 44 |
| Rhodium Rh 45 |
| Paladium Pd 46 |
| Perak Ag 47 |
| Kadmium Cd 48 |
| Lutetium Lu 71 |
| Hafnium Hf 72 |
| Tantalum Ta 73 |
| Tungsten W 74 |
| Renium Re 75 |
| Osmium Os 76 |
| Iridium Ir 77 |
| Platina Pt 78 |
| Emas Au 79 |
| Merkuri Hg 80 |
| Lawrence Lr.103 |
| Rutherfordium RF 104 |
| Dubnium Db 105 |
| Seaborgium Sg 106 |
| Borium Bh 107 |
| Hassiy Hs 108 |
| Meitnerium Gunung 109 |
| Darmstadt DS 110 |
| rontgen Rg 111 |
| Kopernisium Cn 112 |
Metaloid
Metaloid menempati golongan 13-16 pada tabel periodik. Metaloid seperti boron, germanium dan silikon adalah semikonduktor dan digunakan untuk membuat chip komputer dan papan sirkuit.
Tampilkan/Sembunyikan teks
Logam pasca transisi
Elemen disebut logam pasca transisi, termasuk golongan 13-15 tabel periodik. Berbeda dengan logam, mereka tidak bersinar, tetapi memiliki warna matte. Dibandingkan dengan logam transisi, logam pasca transisi lebih lunak dan memiliki lebih banyak suhu rendah meleleh dan mendidih, elektronegativitas lebih tinggi. Elektron valensinya, yang dengannya mereka mengikat unsur-unsur lain, hanya terletak di kulit elektron terluar. Unsur golongan logam pasca transisi memiliki lebih banyak lagi suhu tinggi titik didih dibandingkan metaloid.
Sekarang gabungkan pengetahuan Anda dengan menonton video tentang tabel periodik dan banyak lagi.
Hebat, langkah pertama menuju pengetahuan telah diambil. Sekarang Anda kurang lebih berorientasi pada tabel periodik dan ini akan sangat berguna bagi Anda, karena Sistem Periodik Mendeleev adalah landasan di mana ilmu pengetahuan yang menakjubkan ini berdiri.
Jika Anda merasa tabel periodik sulit dipahami, Anda tidak sendirian! Meskipun sulit untuk memahami prinsip-prinsipnya, mempelajari cara menggunakannya akan membantu Anda ketika mempelajari sains. Pertama, pelajari struktur tabel dan informasi apa yang dapat Anda pelajari darinya tentang setiap unsur kimia. Kemudian Anda bisa mulai mempelajari sifat-sifat setiap elemen. Dan terakhir, dengan menggunakan tabel periodik, Anda dapat menentukan jumlah neutron dalam atom suatu unsur kimia tertentu.
Langkah
Bagian 1
Struktur tabel- Misalnya, baris pertama tabel berisi hidrogen yang memiliki nomor atom 1 dan helium yang memiliki nomor atom 2. Namun letaknya berlawanan karena keduanya berasal dari golongan yang berbeda.
-
Pelajari tentang kelompok yang mengandung unsur-unsur dengan sifat fisik dan kimia yang serupa. Unsur-unsur dari setiap kelompok terletak pada kolom vertikal yang sesuai. Mereka biasanya diidentifikasi dengan warna yang sama, yang membantu mengidentifikasi unsur-unsur dengan sifat fisik dan kimia yang serupa dan memprediksi perilakunya. Semua unsur dalam golongan tertentu mempunyai jumlah elektron yang sama pada kulit terluarnya.
- Hidrogen dapat diklasifikasikan sebagai logam alkali dan halogen. Dalam beberapa tabel ditunjukkan pada kedua kelompok.
- Dalam kebanyakan kasus, kelompok diberi nomor dari 1 hingga 18, dan nomor tersebut ditempatkan di bagian atas atau bawah tabel. Angka dapat ditentukan dalam angka Romawi (misalnya IA) atau Arab (misalnya 1A atau 1).
- Saat berpindah sepanjang kolom dari atas ke bawah, Anda dikatakan sedang “menelusuri grup”.
-
Cari tahu mengapa ada sel kosong di tabel. Unsur-unsur diurutkan tidak hanya berdasarkan nomor atomnya, tetapi juga berdasarkan golongan (unsur-unsur dalam satu golongan mempunyai sifat fisika dan kimia yang serupa). Berkat ini, lebih mudah untuk memahami bagaimana suatu elemen berperilaku. Namun, seiring bertambahnya nomor atom, unsur-unsur yang termasuk dalam golongan yang sesuai tidak selalu ditemukan, sehingga terdapat sel-sel kosong dalam tabel.
- Misalnya, 3 baris pertama memiliki sel kosong karena logam transisi hanya terdapat pada nomor atom 21.
- Unsur-unsur dengan nomor atom 57 sampai 102 diklasifikasikan sebagai unsur tanah jarang, dan biasanya ditempatkan dalam subkelompoknya sendiri di sudut kanan bawah tabel.
-
Setiap baris tabel mewakili suatu periode. Semua unsur pada periode yang sama mempunyai nomor yang sama orbital atom, di mana elektron berada dalam atom. Jumlah orbital sesuai dengan nomor periodenya. Tabel berisi 7 baris, yaitu 7 titik.
- Misalnya, atom unsur periode pertama memiliki satu orbital, dan atom unsur periode ketujuh memiliki 7 orbital.
- Biasanya, periode ditandai dengan angka dari 1 hingga 7 di sebelah kiri tabel.
- Saat Anda bergerak sepanjang garis dari kiri ke kanan, Anda dikatakan sedang “memindai periode”.
-
Belajar membedakan logam, metaloid, dan nonlogam. Anda akan lebih memahami properti suatu elemen jika Anda dapat menentukan jenisnya. Untuk kenyamanan, di sebagian besar tabel, logam, metaloid, dan nonlogam diberi label warna yang berbeda. Logam di sebelah kiri dan nonlogam di sebelah kanan meja. Metaloid terletak di antara mereka.
Bagian 2
Penunjukan elemen-
Setiap elemen ditandai dengan satu atau dua huruf Latin. Biasanya, simbol elemen ditampilkan dalam huruf besar di tengah sel yang sesuai. Simbol adalah nama singkat untuk suatu elemen yang sama di sebagian besar bahasa. Simbol unsur biasanya digunakan saat melakukan eksperimen dan mengerjakan persamaan kimia, jadi mengingatnya akan sangat membantu.
- Biasanya, simbol unsur merupakan singkatan dari nama latinnya, meskipun untuk beberapa unsur, terutama unsur yang baru ditemukan, simbol tersebut berasal dari nama umum. Misalnya, helium dilambangkan dengan simbol He, yang mirip dengan nama umum di sebagian besar bahasa. Pada saat yang sama, besi disebut Fe, yang merupakan singkatan dari nama latinnya.
-
Perhatikan nama lengkap elemen jika diberikan dalam tabel. Elemen "nama" ini digunakan dalam teks biasa. Misalnya, "helium" dan "karbon" adalah nama unsur. Biasanya, meski tidak selalu, nama lengkap unsur tercantum di bawah simbol kimianya.
- Terkadang tabel tidak mencantumkan nama unsur dan hanya memberikan simbol kimianya.
-
Temukan nomor atom. Biasanya, nomor atom suatu unsur terletak di bagian atas sel yang bersangkutan, di tengah, atau di sudut. Itu juga dapat muncul di bawah simbol atau nama elemen. Unsur mempunyai nomor atom dari 1 sampai 118.
- Nomor atom selalu bilangan bulat.
-
Ingatlah bahwa nomor atom berhubungan dengan jumlah proton dalam suatu atom. Semua atom suatu unsur mengandung jumlah proton yang sama. Berbeda dengan elektron, jumlah proton dalam atom suatu unsur tetap konstan. Jika tidak, Anda akan mendapatkan unsur kimia yang berbeda!
-
Tabel periodik, atau tabel periodik unsur kimia, dimulai di pojok kiri atas dan berakhir di akhir baris terakhir tabel (pojok kanan bawah). Unsur-unsur dalam tabel disusun dari kiri ke kanan berdasarkan kenaikan nomor atomnya. Nomor atom menunjukkan berapa banyak proton yang terkandung dalam satu atom. Selain itu, seiring bertambahnya nomor atom, massa atom juga bertambah. Jadi, berdasarkan letak suatu unsur dalam tabel periodik, massa atomnya dapat ditentukan.
Seperti yang Anda lihat, setiap unsur berikutnya mengandung satu proton lebih banyak daripada unsur sebelumnya. Hal ini terlihat jelas jika Anda melihat nomor atom. Nomor atom bertambah satu saat Anda berpindah dari kiri ke kanan. Karena elemen disusun dalam kelompok, beberapa sel tabel dibiarkan kosong.
Bagaimana cara menggunakan tabel periodik?Bagi orang yang belum tahu, membaca tabel periodik sama dengan bagi kurcaci yang melihat rune kuno para elf. Dan tabel periodik, jika digunakan dengan benar, dapat memberi tahu banyak hal tentang dunia. Selain membantu Anda dengan baik dalam ujian, ini juga tidak tergantikan dalam memecahkan sejumlah besar masalah kimia dan fisika. Tapi bagaimana cara membacanya? Untungnya, saat ini semua orang dapat mempelajari seni ini. Pada artikel ini kami akan memberi tahu Anda cara memahami tabel periodik.
Tabel periodik unsur kimia (tabel Mendeleev) adalah klasifikasi unsur kimia yang menetapkan ketergantungan berbagai sifat unsur pada muatan inti atom.
Sejarah Penciptaan Tabel
Dmitry Ivanovich Mendeleev bukanlah seorang ahli kimia sederhana, jika ada yang berpikir demikian. Dia adalah seorang ahli kimia, fisikawan, ahli geologi, ahli metrologi, ahli ekologi, ekonom, pekerja minyak, aeronaut, pembuat instrumen dan guru. Semasa hidupnya, ilmuwan tersebut berhasil banyak melakukan penelitian mendasar di berbagai bidang ilmu pengetahuan. Misalnya, diyakini secara luas bahwa Mendeleev-lah yang menghitung kekuatan ideal vodka - 40 derajat. Kami tidak tahu bagaimana perasaan Mendeleev tentang vodka, tetapi kami tahu pasti bahwa disertasinya dengan topik “Wacana tentang kombinasi alkohol dengan air” tidak ada hubungannya dengan vodka dan mempertimbangkan konsentrasi alkohol dari 70 derajat. Dengan segala kelebihan ilmuwan, penemuan hukum periodik unsur kimia - salah satu hukum dasar alam, memberinya ketenaran terluas.

Ada legenda yang menyatakan bahwa seorang ilmuwan memimpikan tabel periodik, setelah itu yang harus dia lakukan hanyalah menyempurnakan gagasan yang muncul. Tapi, jika semuanya sesederhana itu.. Versi pembuatan tabel periodik ini, rupanya, tidak lebih dari sebuah legenda. Ketika ditanya bagaimana meja dibuka, Dmitry Ivanovich sendiri menjawab: “ Saya sudah memikirkannya mungkin selama dua puluh tahun, tetapi Anda berpikir: Saya sedang duduk di sana dan tiba-tiba... selesai.”
Pada pertengahan abad kesembilan belas, upaya untuk menyusun unsur-unsur kimia yang diketahui (63 unsur diketahui) dilakukan secara paralel oleh beberapa ilmuwan. Misalnya, pada tahun 1862, Alexandre Emile Chancourtois menempatkan unsur-unsur di sepanjang heliks dan mencatat pengulangan siklik sifat-sifat kimia. Ahli kimia dan musisi John Alexander Newlands mengusulkan tabel periodik versinya pada tahun 1866. Fakta menarik adalah ilmuwan tersebut mencoba menemukan semacam harmoni musik mistis dalam susunan unsur-unsurnya. Di antara upaya lainnya, ada juga upaya Mendeleev yang berhasil.

Pada tahun 1869, diagram tabel pertama diterbitkan, dan tanggal 1 Maret 1869 dianggap sebagai hari dibukanya hukum periodik. Inti dari penemuan Mendeleev adalah bahwa sifat-sifat unsur dengan bertambahnya massa atom tidak berubah secara monoton, melainkan secara berkala. Tabel versi pertama hanya berisi 63 elemen, tetapi Mendeleev membuat sejumlah keputusan yang sangat tidak konvensional. Jadi, dia menebak untuk menyisakan ruang di tabel untuk unsur-unsur yang masih belum ditemukan, dan juga mengubah massa atom beberapa unsur. Kebenaran mendasar dari hukum yang diturunkan oleh Mendeleev dikonfirmasi segera, setelah penemuan galium, skandium dan germanium, yang keberadaannya telah diprediksi oleh ilmuwan.
Pandangan modern tentang tabel periodik
Di bawah ini adalah tabelnya sendiri
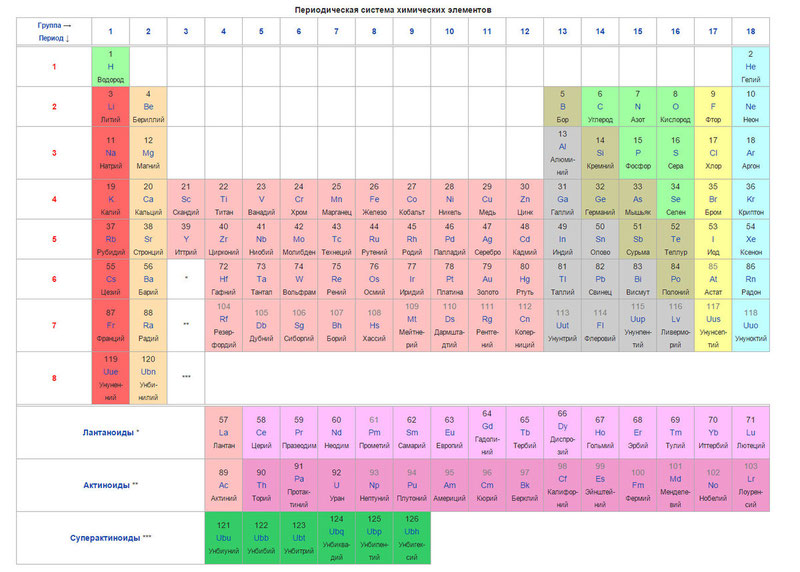
Saat ini, alih-alih berat atom (massa atom), konsep nomor atom (jumlah proton dalam inti) digunakan untuk mengurutkan unsur-unsur. Tabel tersebut berisi 120 unsur, yang disusun dari kiri ke kanan berdasarkan kenaikan nomor atom (jumlah proton)
Kolom tabel mewakili apa yang disebut kelompok, dan baris mewakili periode. Tabel ini memiliki 18 grup dan 8 periode.
- Sifat logam suatu unsur berkurang bila bergerak sepanjang periode dari kiri ke kanan, dan bertambah dalam arah sebaliknya.
- Ukuran atom mengecil ketika bergerak dari kiri ke kanan sepanjang periode.
- Saat Anda berpindah dari atas ke bawah melalui golongan, sifat logam pereduksi meningkat.
- Sifat oksidator dan non-logam meningkat ketika bergerak sepanjang periode dari kiri ke kanan SAYA.
Apa yang kita pelajari tentang suatu elemen dari tabel? Misalnya, mari kita ambil elemen ketiga dalam tabel - litium, dan pertimbangkan secara mendetail.

Pertama-tama, kita melihat simbol elemen itu sendiri dan namanya di bawahnya. Di pojok kiri atas terdapat nomor atom suatu unsur, urutan unsur tersebut disusun dalam tabel. Nomor atom, sebagaimana telah disebutkan, sama dengan jumlah proton dalam inti atom. Jumlah proton positif biasanya sama dengan jumlah elektron negatif dalam suatu atom (kecuali pada isotop).
Massa atom ditunjukkan di bawah nomor atom (dalam tabel versi ini). Jika kita membulatkan massa atom ke bilangan bulat terdekat, kita mendapatkan apa yang disebut nomor massa. Perbedaan antara nomor massa dan nomor atom menunjukkan jumlah neutron dalam inti atom. Jadi, jumlah neutron dalam inti helium adalah dua, dan dalam litium adalah empat.
Kursus kami “Tabel Periodik untuk Boneka” telah berakhir. Sebagai penutup, kami mengundang Anda untuk menonton video tematiknya, dan kami berharap pertanyaan tentang cara menggunakan tabel periodik Mendeleev menjadi lebih jelas bagi Anda. Kami mengingatkan Anda bahwa mempelajari mata pelajaran baru selalu lebih efektif tidak sendirian, tetapi dengan bantuan mentor yang berpengalaman. Itu sebabnya Anda tidak boleh melupakan mereka, yang dengan senang hati akan berbagi pengetahuan dan pengalamannya dengan Anda.
Saat ini secara resmi mengandung 118 bahan kimia. Dari jumlah tersebut, 94 ditemukan di alam, 24 sisanya diperoleh secara buatan reaksi nuklir. Dari semua bahan kimia yang ditemukan di alam, 88; elemen seperti teknesium Tc, prometium Pm, astatin Pada dan Perancis Pdt, serta semua unsur setelah uranium U, diperoleh secara artifisial untuk pertama kalinya. Dalam kondisi normal, zat sederhana yang bersesuaian untuk 11 unsur adalah gas, untuk 2 - cairan, untuk unsur lainnya - padat.
Layak dibaca
 Dmitri Ivanovich Mendeleev- Ilmuwan-ensiklopedis Rusia, tokoh masyarakat. Ahli kimia, ahli kimia fisik, fisikawan, metrologi, ekonom, teknolog, ahli geologi, ahli meteorologi, guru, aeronaut, pembuat instrumen. Profesor Universitas St. Petersburg; Anggota Koresponden dalam kategori “Fisik” dari Akademi Ilmu Pengetahuan Imperial St. Di antara penemuan yang paling terkenal adalah hukum periodik unsur kimia, salah satu hukum dasar alam semesta, yang merupakan bagian integral dari semua ilmu pengetahuan alam.
Dmitri Ivanovich Mendeleev- Ilmuwan-ensiklopedis Rusia, tokoh masyarakat. Ahli kimia, ahli kimia fisik, fisikawan, metrologi, ekonom, teknolog, ahli geologi, ahli meteorologi, guru, aeronaut, pembuat instrumen. Profesor Universitas St. Petersburg; Anggota Koresponden dalam kategori “Fisik” dari Akademi Ilmu Pengetahuan Imperial St. Di antara penemuan yang paling terkenal adalah hukum periodik unsur kimia, salah satu hukum dasar alam semesta, yang merupakan bagian integral dari semua ilmu pengetahuan alam.
Tabel Periodik Unsur Kimia– klasifikasi unsur kimia, menetapkan ketergantungan berbagai sifat unsur pada muatan inti atom. Sistem ini merupakan ekspresi grafis dari hukum periodik yang ditetapkan oleh ahli kimia Rusia D.I. Mendeleev pada tahun 1869. Versi awalnya dikembangkan oleh D.I. Mendeleev pada tahun 1869-1871 dan menetapkan ketergantungan sifat-sifat unsur pada berat atomnya. Secara total, beberapa ratus opsi untuk menggambarkan tabel periodik telah diusulkan. DI DALAM versi modern Sistem ini melibatkan reduksi unsur-unsur menjadi tabel dua dimensi, di mana setiap kolom menentukan sifat fisik dan kimia utama, dan baris-barisnya mewakili periode yang sampai batas tertentu mirip satu sama lain. Pada pertengahan abad ke-19, 63 unsur kimia telah ditemukan, dan upaya untuk menemukan pola dalam kumpulan ini dilakukan berulang kali. Yang lebih umum daripada yang lain adalah 3 bentuk tabel periodik: “pendek”, “panjang” dan “ekstra panjang”. Dalam versi “super panjang”, setiap periode menempati tepat satu baris. Sistem periodik D.I. Mendeleev menjadi tonggak utama dalam perkembangan ilmu atom-molekuler.
