Čak iu školi, sjedeći na satovima kemije, svi se sjećamo stola na zidu učionice ili kemijskog laboratorija. Ova tablica sadržavala je klasifikaciju svih poznatih čovječanstvu kemijski elementi, te temeljne komponente koje čine Zemlju i cijeli Svemir. Tada to nismo mogli ni pomisliti Mendeljejeva tablica nedvojbeno je jedno od najvećih znanstvenih otkrića, koje je temelj našeg suvremenog znanja o kemiji.
Periodni sustav elemenata kemijski elementi D. I. Mendeljejev
Na prvi pogled njezina ideja izgleda varljivo jednostavna: organizirati kemijski elementi redoslijedom povećanja težine njihovih atoma. Štoviše, u većini slučajeva ispada da kemijski i fizička svojstva svaki element je sličan svom prethodnom elementu u tablici. Ovaj obrazac se pojavljuje za sve elemente osim za prvih nekoliko, jednostavno zato što ispred sebe nemaju elemente slične sebi po atomskoj težini. Upravo zahvaljujući otkriću ovog svojstva možemo postaviti linearni niz elemenata u tablicu poput zidnog kalendara i tako kombinirati ogroman broj vrsta kemijskih elemenata u jasnom i koherentnom obliku. Naravno, danas koristimo koncept atomskog broja (broj protona) kako bismo uredili sustav elemenata. To je pomoglo u rješavanju takozvanog tehničkog problema "para permutacija", ali nije dovelo do temeljne promjene u izgledu periodnog sustava.
U periodni sustav elemenata svi elementi poredani su na temelju atomskog broja, elektronske konfiguracije i ponavljanja kemijska svojstva. Redovi u tablici nazivaju se periode, a stupci grupe. Prva tablica, koja datira iz 1869. godine, sadržavala je samo 60 elemenata, no sada se tablica morala povećati kako bi primila 118 elemenata koje danas poznajemo.
Mendeljejev periodni sustav sistematizira ne samo elemente, nego i njihova najraznovrsnija svojstva. Često je kemičaru dovoljno pred očima imati periodni sustav kako bi točno odgovorio na mnoga pitanja (ne samo ispitna, nego i znanstvena).
YouTube ID 1M7iKKVnPJE nije važeći.
Periodični zakon
Postoje dvije formulacije periodični zakon kemijski elementi: klasični i moderni.
Klasična, kako ju je predstavio njen otkrivač D.I. Mendeleev: svojstva jednostavnih tijela, kao i oblici i svojstva spojeva elemenata, periodički ovise o vrijednostima atomskih težina elemenata.
Moderno: svojstva jednostavnih tvari, kao i svojstva i oblici spojeva elemenata, periodički su ovisna o naboju jezgre atoma elemenata (redni broj).
Grafički prikaz periodnog zakona je periodni sustav elemenata, koji je prirodna klasifikacija kemijskih elemenata koja se temelji na pravilnim promjenama svojstava elemenata ovisno o nabojima njihovih atoma. Najčešće slike periodnog sustava elemenata su D.I. Mendeljejevljevi oblici su kratki i dugi.

Grupe i periode periodnog sustava
U grupama nazivaju se okomiti redovi u periodnom sustavu. U skupine se elementi kombiniraju na temelju najvišeg oksidacijskog stanja u njihovim oksidima. Svaka skupina se sastoji od glavne i sekundarne podskupine. Glavne podskupine uključuju elemente malih perioda i elemente velikih perioda s istim svojstvima. Bočne podskupine sastoje se samo od elemenata velikih perioda. Kemijska svojstva elemenata glavne i sporedne podskupine značajno se razlikuju.
Razdoblje naziva vodoravni niz elemenata poredanih prema rastućim atomskim brojevima. U periodnom sustavu postoji sedam razdoblja: prva, druga i treća razdoblja nazivaju se malima, sadrže 2, 8 i 8 elemenata; preostala razdoblja nazivaju se velikima: u četvrtom i petom razdoblju ima 18 elemenata, u šestom - 32, au sedmom (još nije dovršeno) - 31 element. Svaka perioda, osim prve, počinje alkalijskim metalom, a završava plemenitim plinom.
Fizičko značenje serijskog broja kemijski element: broj protona u atomskoj jezgri i broj elektrona koji rotiraju oko atomske jezgre jednaki su atomskom broju elementa.
Svojstva periodnog sustava
Podsjetimo da skupine nazivaju se okomiti redovi u periodnom sustavu i kemijska svojstva elemenata glavne i sporedne podskupine bitno se razlikuju.
Svojstva elemenata u podskupinama prirodno se mijenjaju odozgo prema dolje:
- metalna svojstva se povećavaju, a nemetalna svojstva slabe;
- povećava se atomski radijus;
- povećava se snaga baza i kiselina bez kisika koje stvara element;
- smanjuje se elektronegativnost.
Svi elementi osim helija, neona i argona tvore spojeve kisika; postoji samo osam oblika spojeva kisika. U periodnom sustavu često su prikazani općim formulama, smještenim ispod svake skupine u rastućem redoslijedu oksidacijskog stanja elemenata: R 2 O, RO, R 2 O 3, RO 2, R 2 O 5, RO 3, R2O7, RO4, gdje simbol R označava element ove skupine. Formule viših oksida vrijede za sve elemente skupine, osim u iznimnim slučajevima kada elementi ne pokazuju oksidacijsko stanje jednako broju skupine (npr. fluor).
Oksidi sastava R 2 O pokazuju jaka bazična svojstva, a njihova bazičnost raste s povećanjem atomskog broja, oksidi sastava RO (s izuzetkom BeO) pokazuju bazična svojstva. Oksidi sastava RO 2, R 2 O 5, RO 3, R 2 O 7 pokazuju kisela svojstva, a njihova kiselost raste s povećanjem atomskog broja.
Elementi glavnih podskupina, počevši od IV.skupine, tvore plinovite vodikove spojeve. Postoje četiri oblika takvih spojeva. Oni se nalaze ispod elemenata glavnih podskupina i prikazani su općim formulama u nizu RH 4, RH 3, RH 2, RH.
RH 4 spojevi su neutralne prirode; RH 3 - slabo bazično; RH 2 - blago kiselo; RH - jako kiseli karakter.
Podsjetimo da razdoblje naziva vodoravni niz elemenata poredanih prema rastućim atomskim brojevima.
Unutar razdoblja s povećanjem rednog broja elementa:
- povećava se elektronegativnost;
- metalna svojstva se smanjuju, nemetalna se svojstva povećavaju;
- atomski radijus se smanjuje.

Elementi periodnog sustava
Alkalijski i zemnoalkalijski elementi
To uključuje elemente iz prve i druge skupine periodnog sustava. Alkalijski metali iz prve skupine - mekani metali, srebrne boje, lako se režu nožem. Svi oni imaju jedan elektron u svojoj vanjskoj ljusci i reagiraju savršeno. Zemnoalkalijski metali iz druge skupine također imaju srebrnastu nijansu. Dva elektrona smještena su na vanjskoj razini i, prema tome, ovi metali teže komuniciraju s drugim elementima. U usporedbi s alkalijskim metalima, zemnoalkalijski metali se tope i vriju na višim temperaturama.
Prikaži/sakrij tekst
Lantanidi (elementi rijetkih zemalja) i aktinidi
Lantanidi- skupina elemenata izvorno pronađenih u rijetkim mineralima; otuda i njihov naziv elementi "rijetke zemlje". Naknadno se pokazalo da ovi elementi nisu tako rijetki kao što se u početku mislilo, pa su stoga elementi rijetkih zemalja nazvani lantanidi. Lantanidi i aktinidi zauzimaju dva bloka, koji se nalaze ispod glavne tablice elemenata. Obje skupine uključuju metale; svi lantanidi (osim prometija) su neradioaktivni; aktinoidi su, naprotiv, radioaktivni.
Prikaži/sakrij tekst
Halogeni i plemeniti plinovi
Halogeni i plemeniti plinovi grupirani su u skupine 17 i 18 periodnog sustava elemenata. Halogeni su nemetalni elementi, svi imaju sedam elektrona u svojoj vanjskoj ljusci. U plemeniti plinovi Svi elektroni nalaze se u vanjskoj ljusci, pa gotovo ne sudjeluju u stvaranju spojeva. Ti se plinovi nazivaju "plemenitim" plinovima jer rijetko reagiraju s drugim elementima; to jest, odnose se na pripadnike plemićke kaste koji su tradicionalno izbjegavali druge ljude u društvu.
Prikaži/sakrij tekst
Prijelazni metali
Prijelazni metali zauzimaju skupine 3-12 u periodnom sustavu. Većina ih je gusta, tvrda, dobre električne i toplinske vodljivosti. Njihovi valentni elektroni (pomoću kojih se povezuju s drugim elementima) nalaze se u nekoliko elektronskih ljuski.
Prikaži/sakrij tekst
| Prijelazni metali |
| Skandij Sc 21 |
| Titan Ti 22 |
| Vanadij V 23 |
| Krom Cr 24 |
| Mangan Mn 25 |
| Željezo Fe 26 |
| Cobalt Co 27 |
| Nikal Ni 28 |
| Bakar Cu 29 |
| Cink Zn 30 |
| Itrij Y 39 |
| Cirkonij Zr 40 |
| Niobij Nb 41 |
| Molibden Mo 42 |
| Tehnecij Tc 43 |
| Rutenij Ru 44 |
| Rodij Rh 45 |
| Paladij Pd 46 |
| Srebro Ag 47 |
| Kadmij Cd 48 |
| Lutecij Lu 71 |
| Hafnij Hf 72 |
| Tantal Ta 73 |
| Volfram W 74 |
| Renij Re 75 |
| Osmij Os 76 |
| Iridij Ir 77 |
| Platinasti Pt 78 |
| Zlato Au 79 |
| Merkur Hg 80 |
| Lawrence Lr 103 |
| Rutherfordium Rf 104 |
| Dubnij Db 105 |
| Seaborgium Sg 106 |
| Borium Bh 107 |
| Hassiy Hs 108 |
| Meitnerium Mt 109 |
| Darmstadt Ds 110 |
| Rtg Rg 111 |
| Kopernicij Cn 112 |
Metaloidi
Metaloidi zauzimaju skupine 13-16 periodnog sustava. Metaloidi poput bora, germanija i silicija su poluvodiči i koriste se za izradu računalnih čipova i sklopova.
Prikaži/sakrij tekst
Posttranzicijski metali
Elementi tzv post-prijelazni metali, pripadaju skupinama 13-15 periodnog sustava elemenata. Za razliku od metala, oni nemaju sjaj, ali imaju mat boju. U usporedbi s prijelaznim metalima, postprijelazni metali su mekši i imaju više niske temperature taljenja i vrenja, veća elektronegativnost. Njihovi valentni elektroni, kojima spajaju druge elemente, nalaze se samo na vanjskoj elektronskoj ljusci. Elementi skupine postprijelaznih metala imaju mnogo više visoka temperatura vrelište od metaloida.
Sada učvrstite svoje znanje gledajući video o periodnom sustavu elemenata i više.
Super, prvi korak na putu do znanja je napravljen. Sada ste više-manje orijentirani u periodnom sustavu i to će vam biti vrlo korisno, jer je periodni sustav Mendeljejeva temelj na kojem stoji ova nevjerojatna znanost.
Ako vam je periodni sustav teško razumjeti, niste jedini! Iako može biti teško razumjeti njegova načela, učenje kako ga koristiti pomoći će vam pri proučavanju znanosti. Prvo proučite strukturu tablice i koje informacije iz nje možete saznati o svakom kemijskom elementu. Zatim možete početi proučavati svojstva svakog elementa. I konačno, pomoću periodnog sustava možete odrediti broj neutrona u atomu određenog kemijskog elementa.
Koraci
1. dio
Struktura tablice- Na primjer, prvi redak tablice sadrži vodik, koji ima atomski broj 1, i helij, koji ima atomski broj 2. Međutim, oni se nalaze na suprotnim rubovima jer pripadaju različitim skupinama.
-
Naučite o skupinama koje sadrže elemente sličnih fizikalnih i kemijskih svojstava. Elementi svake skupine nalaze se u odgovarajućem okomitom stupcu. Obično se identificiraju istom bojom, što pomaže u prepoznavanju elemenata sa sličnim fizičkim i kemijskim svojstvima i predviđanju njihovog ponašanja. Svi elementi određene skupine imaju isti broj elektrona u svojoj vanjskoj ljusci.
- Vodik se može klasificirati i kao alkalijske metale i kao halogene. U nekim tablicama naznačeno je u obje skupine.
- U većini slučajeva grupe su označene brojevima od 1 do 18, a brojevi se nalaze na vrhu ili dnu tablice. Brojevi se mogu navesti rimskim (npr. IA) ili arapskim (npr. 1A ili 1) brojevima.
- Kada se krećete po stupcu od vrha prema dolje, kaže se da "pregledavate grupu".
-
Saznajte zašto su u tablici prazna polja. Elementi su poredani ne samo prema svom atomskom broju, već i prema skupini (elementi u istoj skupini imaju slična fizikalna i kemijska svojstva). Zahvaljujući tome, lakše je razumjeti kako se određeni element ponaša. Međutim, kako se atomski broj povećava, elementi koji spadaju u odgovarajuću skupinu nisu uvijek pronađeni, pa u tablici postoje prazna polja.
- Na primjer, prva 3 retka imaju prazne ćelije jer se prijelazni metali nalaze samo od atomskog broja 21.
- Elementi s atomskim brojevima od 57 do 102 klasificirani su kao elementi rijetkih zemalja i obično se nalaze u vlastitoj podskupini u donjem desnom kutu tablice.
-
Svaki redak tablice predstavlja točku. Svi elementi iste periode imaju isti broj atomske orbitale, na kojem se nalaze elektroni u atomima. Broj orbitala odgovara broju perioda. Tablica se sastoji od 7 redaka, odnosno 7 točaka.
- Na primjer, atomi elemenata prve periode imaju jednu orbitalu, a atomi elemenata sedme periode imaju 7 orbitala.
- Razdoblja su u pravilu označena brojevima od 1 do 7 na lijevoj strani tablice.
- Dok se krećete po liniji slijeva nadesno, kaže se da "skenirate razdoblje".
-
Naučiti razlikovati metale, metaloide i nemetale. Bolje ćete razumjeti svojstva elementa ako možete odrediti koji je tip. Radi praktičnosti, u većini tablica označeni su metali, metaloidi i nemetali različite boje. Metali su na lijevoj, a nemetali na desnoj strani stola. Između njih nalaze se metaloidi.
2. dio
Oznake elemenata-
Svaki element označen je jednim ili dva latinična slova. U pravilu je simbol elementa prikazan velikim slovima u sredini odgovarajuće ćelije. Simbol je skraćeni naziv za element koji je isti u većini jezika. Simboli elemenata obično se koriste pri izvođenju eksperimenata i radu s kemijskim jednadžbama, stoga ih je korisno zapamtiti.
- Tipično, simboli elemenata su kratice njihovog latinskog naziva, iako su za neke, posebno nedavno otkrivene elemente, izvedeni iz uobičajenog naziva. Na primjer, helij je predstavljen simbolom He, koji je blizak uobičajenom nazivu u većini jezika. Pritom se željezo označava kao Fe, što je skraćenica njegovog latinskog naziva.
-
Obratite pozornost na puni naziv elementa ako je naveden u tablici. Ovaj element "ime" koristi se u redovnim tekstovima. Na primjer, "helij" i "ugljik" su imena elemenata. Obično, iako ne uvijek, puni nazivi elemenata navedeni su ispod njihovog kemijskog simbola.
- Ponekad tablica ne označava nazive elemenata i daje samo njihove kemijske simbole.
-
Pronađite atomski broj. Obično se atomski broj elementa nalazi na vrhu odgovarajuće ćelije, u sredini ili u kutu. Također se može pojaviti ispod simbola ili naziva elementa. Elementi imaju atomske brojeve od 1 do 118.
- Atomski broj je uvijek cijeli broj.
-
Zapamtite da atomski broj odgovara broju protona u atomu. Svi atomi elementa sadrže isti broj protona. Za razliku od elektrona, broj protona u atomima elementa ostaje konstantan. Inače biste dobili drugačiji kemijski element!
-
Periodni sustav, odnosno periodni sustav kemijskih elemenata, počinje u gornjem lijevom kutu i završava na kraju zadnjeg retka tablice (donji desni kut). Elementi u tablici poredani su s lijeva na desno u rastućem redoslijedu prema njihovom atomskom broju. Atomski broj pokazuje koliko se protona nalazi u jednom atomu. Osim toga, s povećanjem atomskog broja, povećava se i atomska masa. Dakle, prema položaju elementa u periodnom sustavu elemenata, može se odrediti njegova atomska masa.
Kao što vidite, svaki sljedeći element sadrži jedan proton više od elementa koji mu prethodi. To je očito kada pogledate atomske brojeve. Atomski brojevi povećavaju se za jedan kako se pomičete slijeva nadesno. Budući da su elementi raspoređeni u skupine, neke ćelije tablice ostaju prazne.
Kako koristiti periodni sustav?Za neupućenu osobu, čitanje periodnog sustava je isto kao za gnoma koji gleda u drevne rune vilenjaka. A periodni sustav, usput, ako se pravilno koristi, može puno reći o svijetu. Osim što će dobro poslužiti na ispitu, jednostavno je nezamjenjiv u rješavanju ogromnog broja kemijskih i fizikalnih problema. Ali kako to čitati? Srećom, danas svatko može naučiti ovu umjetnost. U ovom članku ćemo vam reći kako razumjeti periodni sustav.
Periodni sustav kemijskih elemenata (Mendeljejevljeva tablica) je klasifikacija kemijskih elemenata koja utvrđuje ovisnost različitih svojstava elemenata o naboju atomske jezgre.
Povijest nastanka Stola
Dmitrij Ivanovič Mendeljejev nije bio običan kemičar, ako netko tako misli. Bio je kemičar, fizičar, geolog, metrolog, ekolog, ekonomist, naftni radnik, aeronaut, instrumentar i učitelj. Tijekom svog života, znanstvenik je uspio provesti mnogo temeljnih istraživanja u različitim područjima znanja. Na primjer, uvriježeno je mišljenje da je Mendeljejev izračunao idealnu jačinu votke - 40 stupnjeva. Ne znamo kako je Mendeljejev mislio o votki, ali pouzdano znamo da njegova disertacija na temu "Rasprava o spoju alkohola s vodom" nije imala nikakve veze s votkom i razmatrala je koncentracije alkohola od 70 stupnjeva. Uz sve zasluge znanstvenika, otkriće periodičnog zakona kemijskih elemenata - jednog od temeljnih zakona prirode, donijelo mu je najširu slavu.

Postoji legenda prema kojoj je jedan znanstvenik sanjao periodni sustav, nakon čega je samo trebao doraditi ideju koja se pojavila. Ali, kad bi sve bilo tako jednostavno.. Ova verzija stvaranja periodnog sustava, očito, nije ništa više od legende. Na pitanje kako je stol otvoren, sam Dmitrij Ivanovič je odgovorio: " Razmišljao sam o tome možda dvadeset godina, ali vi mislite: sjedio sam tamo i odjednom... gotovo je.”
Sredinom devetnaestog stoljeća nekoliko je znanstvenika paralelno pokušavalo složiti poznate kemijske elemente (bila su poznata 63 elementa). Na primjer, 1862. Alexandre Emile Chancourtois postavio je elemente duž spirale i primijetio cikličko ponavljanje kemijskih svojstava. Kemičar i glazbenik John Alexander Newlands predložio je svoju verziju periodnog sustava 1866. godine. Zanimljiva je činjenica da je znanstvenik pokušao otkriti neku vrstu mistične glazbene harmonije u rasporedu elemenata. Između ostalih pokušaja, tu je i Mendeljejevljev pokušaj, koji je okrunjen uspjehom.

Godine 1869. objavljen je prvi tablični dijagram, a 1. ožujka 1869. smatra se danom otvaranja periodičnog zakona. Bit Mendeljejeva otkrića bila je da se svojstva elemenata s povećanjem atomske mase ne mijenjaju monotono, već periodički. Prva verzija tablice sadržavala je samo 63 elementa, ali Mendeljejev je donio niz vrlo nekonvencionalnih odluka. Dakle, pogodio je ostaviti prostor u tablici za još neotkrivene elemente, a također je promijenio atomske mase nekih elemenata. Temeljna ispravnost zakona koji je izveo Mendelejev potvrđena je vrlo brzo, nakon otkrića galija, skandijuma i germanija, čije je postojanje znanstvenik predvidio.
Suvremeni pogled na periodni sustav
Ispod je sama tablica
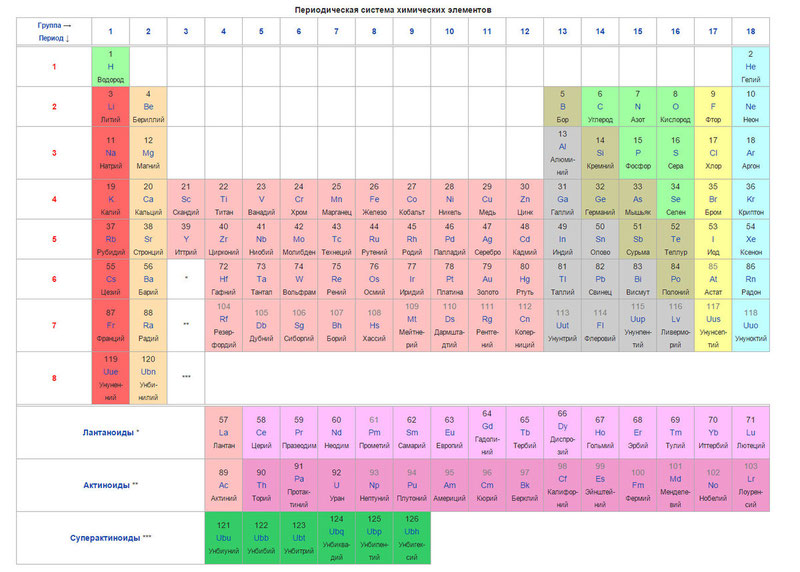
Danas se umjesto atomske težine (atomske mase) za poredak elemenata koristi pojam atomskog broja (broj protona u jezgri). Tablica sadrži 120 elemenata, koji su poredani s lijeva na desno prema rastućem atomskom broju (broju protona)
Stupci tablice predstavljaju takozvane grupe, a reci predstavljaju razdoblja. Tablica ima 18 grupa i 8 perioda.
- Metalna svojstva elemenata opadaju kada se pomiču periodom slijeva nadesno, a povećavaju u suprotnom smjeru.
- Veličine atoma smanjuju se pri pomicanju slijeva nadesno duž perioda.
- Kako se krećete odozgo prema dolje kroz grupu, svojstva redukcijskih metala se povećavaju.
- Oksidirajuća i nemetalna svojstva povećavaju se pomicanjem duž perioda slijeva nadesno ja
Što saznajemo o elementu iz tablice? Na primjer, uzmimo treći element u tablici - litij, i razmotrimo ga detaljno.

Prije svega, vidimo sam simbol elementa i njegovo ime ispod njega. U gornjem lijevom kutu nalazi se atomski broj elementa, kojim je redom element poredan u tablici. Atomski broj, kao što je već spomenuto, jednak je broju protona u jezgri. Broj pozitivnih protona obično je jednak broju negativnih elektrona u atomu (osim u izotopima).
Atomska masa navedena je pod atomskim brojem (u ovoj verziji tablice). Zaokružimo li atomsku masu na najbliži cijeli broj, dobit ćemo ono što se naziva maseni broj. Razlika između masenog broja i atomskog broja daje broj neutrona u jezgri. Tako je broj neutrona u jezgri helija dva, a u litiju četiri.
Završio je naš tečaj Periodical Table for Dummies. Zaključno, pozivamo vas da pogledate tematski video i nadamo se da vam je postalo jasnije pitanje kako koristiti periodni sustav Mendelejeva. Podsjećamo vas da je uvijek učinkovitije proučavati novi predmet ne sami, već uz pomoć iskusnog mentora. Zato nikada ne zaboravite na njih koji će svoje znanje i iskustvo rado podijeliti s vama.
U ovom trenutku službeno sadrži 118 kemikalija. Od toga su 94 pronađena u prirodi, a preostala 24 dobivena su umjetnim putem nuklearne reakcije. Od svih kemikalija pronađenih u prirodi, 88; elementi kao što je tehnecij Tc, prometij Pm, astatin Na i Francuska Fr, kao i svi elementi nakon urana, prvi su put dobiveni umjetnim putem. U normalnim uvjetima, odgovarajuće jednostavne tvari za 11 elemenata su plinovi, za 2 - tekućine, za preostale elemente - čvrste tvari.
Vrijedno čitanja
 Dmitrij Ivanovič Mendeljejev- ruski znanstvenik-enciklopedist, javna osoba. Kemičar, fizikokemičar, fizičar, metrolog, ekonomist, tehnolog, geolog, meteorolog, učitelj, aeronaut, instrumentar. profesor petrogradskog sveučilišta; Dopisni član u kategoriji "fizika" Carske peterburške akademije znanosti. Među najpoznatijim otkrićima je periodični zakon kemijskih elemenata, jedan od temeljnih zakona svemira, sastavni dio cijele prirodne znanosti.
Dmitrij Ivanovič Mendeljejev- ruski znanstvenik-enciklopedist, javna osoba. Kemičar, fizikokemičar, fizičar, metrolog, ekonomist, tehnolog, geolog, meteorolog, učitelj, aeronaut, instrumentar. profesor petrogradskog sveučilišta; Dopisni član u kategoriji "fizika" Carske peterburške akademije znanosti. Među najpoznatijim otkrićima je periodični zakon kemijskih elemenata, jedan od temeljnih zakona svemira, sastavni dio cijele prirodne znanosti.
Periodni sustav kemijskih elemenata– klasifikacija kemijskih elemenata, utvrđivanje ovisnosti različitih svojstava elemenata o naboju jezgre atoma. Sustav je grafički izraz periodičkog zakona koji je ustanovio ruski kemičar D.I. Mendeljejev 1869. godine. Njegovu početnu verziju razvio je D.I. Mendeljejev 1869-1871 i utvrdio ovisnost svojstava elemenata o njihovoj atomskoj težini. Ukupno je predloženo nekoliko stotina opcija za prikaz periodnog sustava. U moderna verzija Sustav uključuje redukciju elemenata u dvodimenzionalnu tablicu, u kojoj svaki stupac definira glavna fizikalna i kemijska svojstva, a redovi predstavljaju razdoblja koja su u određenoj mjeri međusobno slična. Do sredine 19. stoljeća otkrivena su 63 kemijska elementa, a pokušaji da se pronađu uzorci u ovom skupu ponavljani su. Češća od ostalih su 3 oblika periodnog sustava: "kratki", "dugi" i "ekstra-dugi". U "super-dugoj" verziji svaka točka zauzima točno jedan redak. Periodni sustav D.I. Mendeljejev je postao velika prekretnica u razvoju atomsko-molekularne znanosti.
